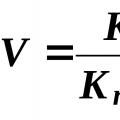В чешмяна вода
Цел на работата: да се научи как да се определя концентрацията на остатъчен активен хлор в чешмяната вода.
Основни теоретични положения
Хлорът може да съществува във вода в състава на хлориди и такива съединения като: свободен хлор (Cl 2), хипохлоритен анион (ClO -), хипохлорна киселина (HClO), хлорамини (монохлорамин NH 2 Cl, дихлорамин NHCl 2, азотен трихлорид NCl 3 ) ...
Общото съдържание на тези съединения се нарича терминът "активен хлор". Активният хлор се предлага в две форми: свободен хлор и комбиниран хлор. Свободен хлор - хлорът, присъстващ във водата като хипохлорна киселина, хипохлоритен йон или разтворен елементарен хлор. Свързан хлор - Хлор, който присъства във водата като хлорамини. Общият хлор е сумата от свободен и комбиниран хлор. Хлорамините са производни на амоняк, образувани при замяната на един, два или три водородни атома с хлорни атоми.
Съединенията, съдържащи активен хлор, се използват за дезинфекция (дезинфекция) на питейна вода и вода в плувни басейни, химическо третиране на някои отпадъчни води, елиминиране на огнища на разпространение на инфекциозно замърсяване (например белина).
Най-широко използваният за дезинфекция на питейната вода е свободният хлор, който при разтваряне във вода се диспропорционира според реакцията
Cl2 + H2O = H + + Cl - + HOCl
Ефектът на хлора върху микроорганизмите зависи от първоначалната доза хлор, продължителността на съхранението му във вода и рН на водата. Хлорът се изразходва при окисляването на органични и неорганични примеси.
Когато избирате дезинфектант, трябва да вземете предвид съдържанието на "активен хлор" в него. "Активно" се отнася до количеството молекулен хлор, съответстващо на окислителната способност на дадено съединение спрямо калиев йодид в кисела среда. Концепцията за "активен хлор" не определя истинското съдържание на хлор в съединението, а окислителната способност на съединението в кисела среда за калиев йодид.
В естествената вода не се допуска съдържанието на "активен хлор"; в питейната вода, нейната максимално допустима концентрация (MPC) се определя по отношение на хлор, на ниво 0,3-0,5 mg / l в свободна форма и на ниво от 0,8-1,2 mg / l в свързана форма.
"Активният хлор" присъства в питейната вода за не повече от няколко десетки минути и се отстранява напълно дори при краткосрочно кипене на водата. Поради тази причина анализът на избраната проба за съдържанието на активен хлор трябва да се извърши незабавно.
Същността на метода
Активният хлор се определя по йодометричен метод (метод на йодометрично титруване). Методът се основава на свойството на всички съединения, съдържащи активен хлор в кисела среда, да изолират свободния йод от калиев йодид
Cl 2 + 2I - = I 2 + 2Cl -
ClO - + 2H + + 2I - = I 2 + Cl - + H 2 O
HClO + H + + 2I - = I 2 + Cl - + H 2 O
NH 2 Cl + 2H + + 2I - = I 2 + NH 4 + + Cl -
Свободният йод се титрува с разтвор на натриев тиосулфат в присъствието на нишесте, което се добавя за по-точно определяне на точката на еквивалентност. Озон, нитрити, железен оксид и други съединения в кисел разтвор освобождават йод от калиев йодид; следователно водните проби се подкисляват с буферен разтвор с рН 4,5.
Йодометричният метод е предназначен за анализ на вода със съдържание на активен хлор над 0,3 mg / l. Методът може да се използва за анализ на мътна и оцветена вода.
Съдове, реактиви
Конична колба със запушалка 250 ml, мерителен цилиндър 100 ml, бюретка 25 ml, микробюрета 5 ml, пипета 1 ml, фуния
Ацетатен буферен разтвор (рН 4,5), калиев йодид в кристали, разтвор на натриев тиосулфат (натриев сулфат) (0,01 N и 0,005 N), разтвор на калиев дихромат (0,01 N), сярна киселина (25%), разтвор на нишесте (0,5%), дестилирана вода
Работна поръчка
1. Определяне на корекционния коефициент
В конична колба поставете 0,5 g калиев йодид, разтворете в 2 ml дестилирана вода, добавете 5 ml сярна киселина (25%), след това 10 ml 0,01 N. разтвор на калиев дихромат, добавете 80 ml дестилирана вода, затворете колбата със запушалка, разбъркайте и поставете на тъмно място за 5 минути. Освободеният йод се титрува с натриев тиосулфат в присъствието на 1 ml добавено нишесте в края на титруването.
2. Определяне на остатъчен активен хлор
Изсипете 0,5 g калиев йодид в конична колба, разтворете го в 1-2 ml дестилирана вода, след това добавете 1 ml буферен разтвор и след това добавете 250 ml анализирана вода. Освободеният йод се титрува с 0,005 N. разтвор на натриев тиосулфат от микробюрета до получаване на светложълт цвят, след което се добавя 1 ml 0,5% разтвор на нишесте и разтворът се титрува до изчезване на синия цвят. Разделенията на микробюретата определят общия обем тиосулфат, изразходван за титруване (както преди, така и след добавянето на нишесте).
Обработка на резултатите
1. Коефициентът на корекция (0,01; 0,005 N. разтвори на натриев сулфат) се изчислява по формулата
където е количеството на натриевия сулфат, изразходвано за титруване, ml.
2. Концентрацията на остатъчния активен хлор (mg/l) се изчислява по формулата
![]()
където V T е сумата от 0,005 n. разтвор на натриев тиосулфат, изразходван за титруване, ml; K е корекционният коефициент за нормалността на разтвора на натриев тиосулфат; 0,177 - съдържанието на активен хлор в mg, съответстващо на 1 ml 0,005 N. разтвор на тиосулфат; 1000 - коефициент на преобразуване на мерните единици от милилитри в литри; V A - обем на водната проба, взета за анализ, мл.
Представяне на резултатите
Получените резултати са записани в таблица 1.1.
Таблица 1.1
Експериментални данни
Въпроси за самотест
1. Защо е необходимо да се хлорира водата?
2. Какви съединения могат да съдържат хлор във водата?
3. Какво е “активен” хлор, “свободен” и “свързан” хлор?
4. Същността на метода на йодометрично титруване при определяне на "активния" хлор?
5. Максимално допустима концентрация на "активен" хлор в питейната вода?
6. Допустимо ли е съдържанието на "активен" хлор в естествената вода?
7. Защо анализът на избраната проба за съдържание на "активен" хлор трябва да се извърши незабавно?
Лабораторна работа No2.
Йодометричен метод
Методът се основава на окисляването на йодида с активен хлор до йод, който се титрува с натриев тиосулфат. Оксидите, съдържащи се във водата, отделят йод от калиев йодид, поради което водните проби се подкисляват с буферен разтвор с рН 4,5.
Йодометричният метод е предназначен за анализ на вода със съдържание на активен хлор над 0,3 mg / l. Методът може да се използва и за оцветени и мътна вода.
· Калиев йодид KJ по ГОСТ 4232, 10% воден разтвор.
· Натриев сулфат (натриев тиосулфат) Na 2 S 2 O 3 воден съгласно TU 6-09-2540, 0,005 n разтвор.
Ацетатна буферна смес
· Водоразтворимо нишесте в съответствие с GOST 10163, 0,5% разтвор, приготвен в съответствие с GOST 4919.1.
Бюретка с кран
напредък
В 3 конични колби със смляна запушалка с вместимост 250 ml добавете:
100 мл анализирана чешмяна вода
5 ml 10% разтвор на калиев йодид
· 5 ml ацетатна буферна смес.
Съдържанието на колбата се смесва. Освободеният йод се титрува с 0,005 N. разтвор на натриев сулфат до светложълт цвят, след което се добавя 1 ml 0,5% разтвор на нишесте и разтворът се титрува до изчезване на синия цвят.
Въведете резултатите в таблицата
Обработка на резултатите.
Концентрацията на C ax в mg / l се изчислява по формулата:
където: V- среден обем 0,005 n. разтвор на натриев сулфат, изразходван за титруване на водна проба, ml; н- еквивалентната концентрация на работния разтвор на натриев сулфат; 35,45 - еквивалентна маса на хлора, V в- обемът на анализираната водна проба, мл.
Като резултат от анализа се взема средноаритметичната стойност на три паралелни определяния.
За лабораторни техници
1. Приготвяне на 10% разтвор на калиев йодид: 10 g калиев йодид се разтварят в 90 ml прясно приготвена и охладена дестилирана вода.
2. Приготвяне на буферен разтвор: 102 1М оцетна киселина (60 g оцетна киселина в 1 l вода) и 98 1M разтвор на натриев ацетат (136,1 g натриев ацетат в 1 l вода) се изсипват в 1 L мерителна колба и доведен до знака с дестилирана вода.
3. Приготвяне на 0,1 N разтвор на разтвор на натриев сулфат: 25 g натриев тиосулфат се разтварят в дестилирана вода, прибавят се 0,2 g натриев карбонат (Na 2 CO 3), обемът се довежда до 1 литър. Приготвяне на 0,005 N разтвор на натриев сулфат: 50 ml 0,1 N разтвор на натриев тиосулфат се разреждат с дестилирана вода, прибавят се 0,2 g натриев карбонат (Na2CO3). доведете обема до 1 литър.
Определяне на свободния остатъчен хлор чрез титруване с метилоранж
Методът се основава на окисляването на метилоранжа със свободен хлор, за разлика от хлорамините, чийто окислителен потенциал е недостатъчен за унищожаване на метилоранжа.
Използвани реактиви и оборудване.
· Конични колби със смлени капаци с вместимост 250 ml.
· Солна киселина съгласно GOST 3118-67 с плътност 1,19 g / cm 3.
Метилово оранжево в съответствие с GOST 10816-64
· Дестилирана вода в съответствие с GOST 6709-72.
Бюретка с кран
Приготвяне на 0,005-силов разтвор на метилоранж: 50 mg метилоранж се разтварят в дестилирана вода, довежда се до обем от 1 литър. 1 ml от този разтвор съответства на 0,0217 mg свободен хлор.
Приготвяне на 5 N разтвор на солна киселина: дестилирана вода се излива в мерна колба, след което бавно се добавят 400 ml солна киселина и се довежда до 1 литър с дестилирана вода.
напредък
1. Напълнете бюретата с 0,005 N разтвор на метил оранжево.
2. Отмерете 100 ml от анализираната вода в 3 колби в мерителен съд.
3. Добавете 2-3 капки 5 N разтвор на солна киселина в една от колбите с анализираната вода, разбъркайте.
4. Бързо титрувайте водата с разтвор на метилоранжев, докато се появи устойчив розов цвят.
5. Повторете стъпки 3 и 4 за двете останали колби с анализираните проби.
6. Въведете получените данни в таблицата
Обработка на резултатите
![]()
където V mo е обемът на разтвора на метилово оранжево, изразходван за титруване, ml;
0,0217 - титър на разтвора на метил оранжево;
0,04 - емпиричен коефициент;
V in - обемът на водата, взета за анализ, ml
Направете заключение за съответствието на получената концентрация на остатъчен хлор във вода на MPC GOST 2874-82
3. Тестови въпроси
GOST 18190-72
МЕЖДУДЪРЖАВЕН СТАНДАРТ
ПИЯ ВОДА
МЕТОДИ ЗА ОПРЕДЕЛЯНЕ СЪДЪРЖАНИЕТО НА ОСТАТЪЧЕН АКТИВЕН ХЛОР
Официално издание
Стандартинформ
МЕЖДУДЪРЖАВЕН СТАНДАРТ
ПИЯ ВОДА
Методи за определяне съдържанието на остатъчен активен хлор
Пия вода. Методи за определяне на остатъчното съдържание на хлор
ISS 13.060.20
Дата на въвеждане 01.01.74
Този стандарт се прилага за питейната вода и определя методи за определяне на съдържанието на остатъчен активен хлор.
1. МЕТОДИ ЗА ВЗЕМАНЕ НА ПРОБИ
1.1. Водните проби се вземат в съответствие с GOST 24481 * и GOST 2874 **.
1.2. Обемът на водната проба за определяне на съдържанието на активен хлор не трябва да бъде по-малък от 500 cm 3.
1.3. Водни проби не са запазени. Определянето трябва да се извърши веднага след вземането на пробата.
2. ЙОДОМЕТРИЧЕН МЕТОД
2.1. Същността на метода
Методът се основава на окисляването на йодида с активен хлор до йод, който се титрува с натриев тиосулфат. Озон, нитрити, железен оксид и други съединения в кисел разтвор освобождават йод от калиев йодид; следователно водните проби се подкисляват с буферен разтвор с рН 4,5.
Йодометричният метод е предназначен за анализ на вода със съдържание на активен хлор над 0,3 mg / dm 3 с обем на пробата 250 cm 3. Методът може да се препоръча и за цветни и мътна вода.
2.2. Оборудване, материали и реактиви
Лабораторни стъклени съдове в съответствие с GOST 1770, GOST 29169 и GOST 29251, с вместимост: мерни колби 100 и 1000 cm 3; пипети без деления 5, 10, 25 cm 3; бюретка с кран 25, 50 см 3; микробюрета 5 см 3.
Конични колби със смлени запушалки с вместимост 250 cm 3 в съответствие с GOST 25336.
Калиев йодид в съответствие с GOST 4232, x. часа, в кристали.
* На територията на Руската федерация е в сила GOST R 51593-2000.
** На територията на Руската федерация е в сила GOST R 51232-98.
Препечатването е забранено
© СТАНДАРТИНФОРМ, 2009
Официално издание ★
Хлороформ (трихлорометан).
Салицилова киселина.
Ледена оцетна киселина съгласно GOST 61.
Калиев дихромат съгласно GOST 4220.
Сярна киселина в съответствие с GOST 4204.
Разтворимо нишесте съгласно GOST 10163.
Кристален натриев карбонат в съответствие с GOST 84.
Натриев сулфат (натриев тиосулфат) в съответствие с GOST 27068.
Всички реагенти, използвани в анализа, трябва да бъдат с квалификация "аналитичен клас" (аналитичен клас).
2.3. Подготовка за анализ
2.3.1. Готвене 0,1 N. разтвор на натриев сулфат
25 g натриев тиосулфат Na 2 S 2 0 3 5H 2 0 се разтварят в прясно преварена и охладена дестилирана вода, добавя се 0,2 g натриев карбонат (Na 2 C0 3) и обемът се довежда до 1 dm 3.
2.3.2. Препарат 0,01 N. разтвор на натриев сулфат
100 cm 3 0,1 N. Разтворът на натриев тиосулфат се разрежда с прясно преварена и охладена дестилирана вода, добавя се 0,2 g натриев карбонат и разтворът се довежда до 1 dm 3. Разтворът се използва, когато съдържанието на активен хлор в пробата е повече от 1 mg / dm 3.
2.3.3. Готвене 0,005 N. разтвор на натриев сулфат
50 cm 3 0,1 N. Разтворът на натриев тиосулфат се разрежда с прясно преварена и охладена дестилирана вода, добавя се 0,2 g натриев карбонат и разтворът се довежда до 1 dm 3. Разтворът се използва, когато съдържанието на активен хлор в пробата е по-малко от 1 mg / dm 3.
2.3.4. Препарат 0,01 N. разтвор на калиев бихромат
0,4904 g калиев бихромат K 2 Cr 2 0 7, претеглен с точност ± 0,0002 g, прекристализиран и изсушен при 180 ° C до постоянно тегло, се разтваря в дестилирана вода и обемът се довежда до 1 dm 3.
2.3.5. Приготвяне на 0,5% разтвор на нишесте
0,5 g разтворимо нишесте се смесва с малко количество дестилирана вода, изсипва се в 100 cm 3 вряща дестилирана вода и се вари няколко минути. След охлаждане се консервира чрез добавяне на хлороформ или 0,1 g салицилова киселина.
2.3.6. Приготвяне на буферен разтвор pH 4.5
102 cm 3 1 M оцетна киселина (60 g ледена оцетна киселина в 1 dm 3 вода) и 98 cm 3 1 M разтвор на натриев ацетат (136,1 g натриев ацетат CH 3 COONa ZN 2 0 в 1 dm 3 вода) се изсипват в обемна колба с вместимост 1 dm 3 и доведена до маркировката с дестилирана вода (предварително сварена и охладена до 20 ° C, без въглероден диоксид).
2.3.7. Коефициент на корекция 0,01 N. разтвор на натриев сулфат се определя с 0,01 N. разтвор на калиев дихромат, както следва: в конична колба със смляна запушалка поставете 0,5 g калиев йодид, тестван за отсъствие на йод, разтворете в 2 cm 3 дестилирана вода, добавете 5 cm 3 сярна киселина (1: 4), след това 10 cm 3 0 , 01 N. разтвор на калиев дихромат, добавете 80 cm 3 дестилирана вода, затворете колбата със запушалка, разбъркайте и поставете на тъмно място за 5 минути. Освободеният йод се титрува с натриев тиосулфат в присъствието на 1 cm 3 добавено нишесте в края на титруването.
2.3.8. Корекционният фактор (K) (0,01; 0,005 N. разтвори на натриев сулфат) се изчислява по формулата
където v е количеството натриев сулфат, изразходвано за титруване, cm 3.
2.4. Анализ
0,5 g калиев йодид се изсипва в конична колба, разтваря се в 1-2 cm 3 дестилирана вода, след което се добавя буферен разтвор в количество, приблизително равно на една и половина алкалност на анализираната вода, след което 250-500 cm 3 анализирана вода се добавя. Освободеният йод се титрува с 0,005 N. разтвор на натриев тиосулфат от микробюрета, докато се появи светложълт цвят, след което се добавя 1 cm 3 от 0,5% разтвор на нишесте и разтворът се титрува до изчезване на синия цвят. При определяне на алкалността водата се дехлорира предварително с натриев тиосулфат в отделна проба.
Когато концентрацията на активен хлор е по-малка от 0,3 mg, се вземат големи обеми вода за титруване.
2.5. Обработка на резултатите
y - K-0,177 ■ 1000
л у,
където y е сумата от 0,005 n. разтвор на натриев тиосулфат, използван за титруване, cm 3;
K е корекционният коефициент за нормалността на разтвора на натриев тиосулфат;
V е обемът на водната проба, взета за анализ, cm 3.
3. МЕТОД ЗА ОПРЕДЕЛЯНЕ НА СВОБОДЕН ОСТАТЪЧЕН ХЛОР ЧРЕЗ ТИТРУВАНЕ С МЕТИЛОВ Оранжев
3.1. Същността на метода
Методът се основава на окисляването на метилоранжа със свободен хлор, за разлика от хлорамините, чийто окислителен потенциал е недостатъчен за унищожаване на метилоранжа.
3.2. Оборудване, материали, реактиви
Лабораторни стъклени съдове в съответствие с GOST 1770 и GOST 29251, с вместимост: мерни колби 100 и 1000 cm 3; микробюрета с кран 5 см 3. Капкомер в съответствие с GOST 25336.
Порцеланови изпарителни чаши в съответствие с GOST 9147.
Солна киселина съгласно GOST 3118, с плътност 1,19 g / cm 3.
Метилов оранжев (натриева пара-диметиламиноазобензенсулфонова киселина) съгласно TU 6-09-5171.
Дестилирана вода в съответствие с GOST 6709.
3.3. Подготовка за анализ
3.3.1. Приготвяне на 0,005% разтвор на метил оранжево
50 mg метил портокал се разтварят в дестилирана вода в мерна колба и се довежда до 1 dm 3 с дестилирана вода. 1 cm 3 от този разтвор съответства на 0,0217 mg свободен хлор.
3.3.2. Готвене 5 N. разтвор на солна киселина
Дестилирана вода се излива в мерителна колба, след което бавно се добавят 400 cm 3 солна киселина HC1 и се довежда с дестилирана вода до 1 dm 3.
3.4. Анализ
100 cm 3 от анализираната вода се поставят в порцеланова чаша, добавят се 2-3 капки 5 N. разтвор на солна киселина и при разбъркване се титрува бързо с разтвор на метилоранжево, докато се появи неизчезващ розов цвят.
3.5. Обработка на резултатите
0,04 + (v- 0,0217) ■ 1000
където V е количеството 0,005% разтвор на метил оранжево, изразходено за титруване, cm 3,
0,0217 - титър на разтвора на метил оранжево;
0,04 - емпиричен коефициент;
V е обемът на водата, взета за анализ, cm "
Чрез разликата между съдържанието на общ остатъчен хлор, определено по йодометричен метод, и съдържанието на свободен остатъчен хлор, определено чрез титруване с метилоранжев, се установява съдържанието на хлораминов хлор (X 2):
x 2 = x-x 1.
4. МЕТОД ЗА ОТДЕЛНО ОПРЕДЕЛЯНЕ НА СВОБОДЕН ХЛОР, МОНОХЛОРАМИН НА СВЪРЗВАНЕ И ДИХЛОРАМИН ПО МЕТОДА НА ПЕЙЛИН
4.1. Същността на метода
Методът се основава на способността на различните видове хлор да превръщат при определени условия редуцираната безцветна форма на диетилпарафенилендиамин в полуокислена оцветена форма, която отново се редуцира до безцветна с двувалентни железни йони. Серия от титрувания с разтвор на сол на Мор се използва за определяне на свободен хлор, монохлорамин и дихлорамин в присъствието на диетилпарафенилендиамин като индикатор. Свободният хлор образува индикаторен цвят в отсъствието на калиев йодид, монохлораминът дава цвят в присъствието на много малки количества калиев йодид (2-3 mg), а дихлораминът образува цвят само в присъствието на големи количества KI (около 1 g) и когато разтворът престои 2 минути ... Количеството на разтвора на сол на Мор, изразходвано за титруване, определя съдържанието на този вид активен хлор, поради което се образува оцветената форма на индикатора.
4.2. Оборудване, материали, реактиви
Лабораторни стъклени съдове съгласно GOST 1770 и GOST 29251,
вместимост: мерни колби 100 и 1000 cm 3; градуирани цилиндри 5 и 100 cm 3; микробюрети 1 и 2 см 3.
Конични колби с вместимост 250 cm 3; колби от тъмно стъкло с вместимост 100-200 см 3.
Двойна сулфатна сол на железен оксид и амоний (сол на Мор) в съответствие с GOST 4208.
Калиев йодид съгласно GOST 4232.
Калиев фосфат монозаместен съгласно GOST 4198, x. з.
Сярна киселина в съответствие с GOST 4204.
Безводен двуосновен натриев фосфат безводен съгласно GOST 11773.
Трилон В (комплексон III, динатриева сол на етилендиаминтетраоцетна киселина) съгласно GOST 10652.
Дестилирана вода в съответствие с GOST 6709.
Диетил парафенилендиамин оксалат или сулфат.
Всички реагенти, използвани за анализ, трябва да бъдат с квалификация "аналитична степен" (аналитична степен).
4.3. Подготовка за анализ
4.3.1. Приготвяне на стандартен разтвор на сол на Мор
1,106 g сол на Мор Fe (NH 4) 2 (S0 4) 2 * 6H 2 0 се разтваря в дестилирана вода, подкислява се с 1 cm 3 от 25% разтвор на сярна киселина H 2 S0 4 и се довежда до 1 dm 3 с прясно преварена и охладена дестилирана вода... 1 cm 3 от разтвора съответства на 0,1 mg активен хлор. Ако определянето се извършва в 100 cm 3 вода, тогава количеството кубични сантиметри сол на Мор, изразходвано за титруване, съответства на mg / dm 3 хлор или монохлорамин, или дихлорамин. Разтворът е стабилен за един месец. Съхранявайте го на тъмно място.
4.3.2. Фосфатен буфериран физиологичен разтвор
Към 2,4 g дизаместен натриев фосфат Na 2 HP0 4 и 4,6 g мономегенен калиев фосфат KN 2 P0 4 се добавят 10 cm 3 от 0,8% разтвор на Trilon B и се довежда с дестилирана вода до 100 cm 3.
4.3.3. Приготвяне на индикатора диетилпарафенилендиамин (оксалат или сулфат) 0,1% разтвор
0,1 g диетил парафенилендиамин оксалат (или 0,15 g сулфат) се разтварят в 100 cm 3 дестилирана вода с добавяне на 2 cm 3 от 10% разтвор на сярна киселина. Индикаторният разтвор трябва да се съхранява в бутилка от тъмно стъкло.
4.4. Анализ
4.4.1. Определяне на съдържанието на свободен хлор
В конична колба за титруване се поставят 5 cm 3 фосфатен буферен разтвор, 5 cm 3 разтвор на диетил парафенилендиамин оксалат или сулфат и се добавят 100 cm 3 анализирана вода, разтворът се разбърква. В присъствието на свободен хлор разтворът става розов; бързо се титрува от микробюрета със стандартен разтвор на сол на Мор до изчезване на цвета, като се разбърква енергично. Консумацията на сол на Мор за титруване (A, cm 3) съответства на съдържанието на свободен хлор, mg / dm 3.
Ако анализираната вода съдържа значителни количества свободен хлор (повече от 4 mg / dm 3), за анализ трябва да се вземат по-малко от 100 cm 3 вода, тъй като големи количества активен хлор могат напълно да унищожат индикатора.
4.4.2. Определяне на съдържанието на монохлорамин
Към колбата с титрувания разтвор се добавя кристал (2-3 mg) йод
добавяне на калий, разтворът се разбърква. В присъствието на монохлорамин моментално се появява розов цвят, който веднага се титрува със стандартен разтвор на сол на Мор. Количеството кубични сантиметри сол на Мор, използвано за титруване (B, cm 3), съответства на съдържанието на монохлорамин, mg / dm 3.
4.4.3. Определяне на съдържанието на дихлорамин
След определяне на съдържанието на монохлорамин, към титрувания разтвор отново се добавя около 1 g калиев йодид, разбърква се, докато солта се разтвори и разтворът се оставя да престои 2 минути. Появата на розов цвят показва наличието на дихлорамин във водата. Разтворът се титрува със стандартен разтвор на сол на Мор до изчезване на цвета. Консумацията на сол на Мор (C, cm 3) съответства на съдържанието на дихлорамин, mg / dm 3.
4.5. Обработка на резултатите
X b = A + B + C,
ИНФОРМАЦИОННИ ДАННИ
1. ОДОБРЕН И ВЪВЕДЕН В СИЛА с Постановление на Държавния комитет по стандартите на Министерския съвет на СССР от 25.10.72 г. № 1967 г.
2. ВЪВЕДЕН ЗА ПЪРВИ ПЪТ
3. РЕФЕРЕНТНИ НОРМАТИВНИ И ТЕХНИЧЕСКИ ДОКУМЕНТИ
|
Номер на артикул |
Номер на артикул |
||
|
GOST 9147-80 | |||
|
GOST 10163-76 | |||
|
ГОСТ 1770-74 |
GOST 10652-73 | ||
|
GOST 2874-82 |
GOST 11773-76 | ||
|
GOST 3118-77 |
GOST 24481-80 | ||
|
GOST 4198-75 |
GOST 25336-82 | ||
|
GOST 4204-77 |
GOST 27068-86 | ||
|
GOST 4208-72 |
GOST 29169-91 | ||
|
GOST 4220-75 |
GOST 29251-91 | ||
|
GOST 4232-74 |
ТУ 6-09-5171-84 | ||
|
GOST 6709-72 |
Остатъчен хлор- оставащ хлор във водата след приложената доза и след окисляването на веществата във водата. Той може да бъде Безплатнои обвързани, т.е. представени от различни форми на хлор. Именно остатъчният хлор е индикатор за достатъчността на приетата доза хлор. Съгласно изискванията на SanPiN 2.1.4.1074-01, концентрацията на остатъчен хлор във водата, преди да влезе в мрежата, трябва да бъде в диапазона от 0,3 - 0,5 mg / l.
28. Определете нуждата от хлор във водата чрез хлориране на вода в три чаши.
Нуждата от хлорна водае количеството активен хлор (в милиграми), необходимо за ефективна дезинфекция на 1 литър вода и осигуряване на остатъчен свободен хлор в диапазона от 0,3-0,5 mg/l след 30-минутен контакт с вода, или количеството на остатъчния свободен хлор комбиниран хлор в рамките на 0,8-1,2 mg след 60 минути контакт. За да се определи необходимата доза хлор по време на хлориране с нормални дози, се извършва пробно хлориране на водата. На полето се извършва пробно хлориране в три чаши, във всяка от които се наливат 200 ml вода за изпитване, поставят се стъклени пръчки и с помощта на проверена пипета (25 капки са равни на 1 ml) 1% разтвор от белина се добавя: в първата - 1 капка, във втората - 2 капки, в третата - 3 капки. Водата в чашите се разбърква добре и след 30 минути се установява наличието на остатъчен хлор в нея. За да направите това, добавете 2 ml 5% разтвор на калиев йодид, 2 ml солна киселина (1: 5), 1 ml 1% разтвор на нишесте към всяка чаша и разбъркайте добре. При наличие на остатъчен хлор водата става синя, колкото по-интензивна, толкова повече остатъчен хлор съдържа. Интензитетът на цвета съответства на следните концентрации на остатъчен хлор във вода: леко синьо (0,1 mg / l), светло синьо (0,2 mg / l), синьо (0,3 mg / l), наситено синьо (0,5 mg / l); синьо-черен (дъното на епруветката не се вижда) - 1,0 mg / l и повече.
Водата в чаши, където се появи син цвят, се титрува на капки с 0,7% разтвор на натриев тиосулфат до обезцветяване, като се разбърква след добавяне на всяка капка.
За да изчислите дозата, изберете стъклото, където е настъпило обезцветяване от 2 капки натриев тиосулфат, тъй като съдържанието на остатъчен хлор в това стъкло е 0,4 mg / l (1 капка 0,7% разтвор на натриев тиосулфат свързва 0,04 mg хлор, което съответства на преобразувано в 1 литър 0,04x5 = 0,2 mg / l). Ако е настъпило обезцветяване от 1 капка, съдържанието на остатъчен хлор е недостатъчно - 0,2 mg / l; с обезцветяване от 3 капки, съдържанието на остатъчен хлор е прекомерно - 0,6 mg / l.
В зависимост от резултатите от пробното хлориране се изчислява количеството белина, необходимо за хлорирането на 1 литър вода.
29. Демонстрирайте метода за вземане на проби от въздуха с цел изследване на бактериалното замърсяване на въздуха.
Съществуват два основни метода за вземане на проби от въздуха за изследване: 1) утаяване – основава се на механичното утаяване на микроорганизми; 2) аспирация - базирана на активно засмукване на въздух (този метод дава възможност да се определи не само качественото, но и количественото съдържание на бактериите).
Метод на утаяване
Паничките на Петри с хранителна среда (MPA) се поставят хоризонтално отворени, на различни нива от пода. Методът се основава на механичното утаяване на бактерии върху повърхността на агара в петриевите блюда. Плаките със средата се излагат за 10 до 20 минути, в зависимост от очакваното замърсяване на въздуха. За идентифициране на патогенна флора се използват избираеми среди. Експозицията в тези случаи се удължава до 2-3 ч. След експозицията съдовете се затварят, доставят се в лабораторията и се поставят в термостат за 24 часа при 37°С. На следващия ден се изследват порасналите колонии. Този метод се използва главно в затворени помещения.
(Метод на аспирация)
Речменски бактериологичен капан. Преди работа устройството се напълва със стерилна сода. Работата на устройството се основава на изтегляне на въздух през него с помощта на аспиратор. Това разпръсква течността в устройството. След края на засмукването течността, през която е пропуснат въздухът, се инокулира при 0,1-0,2 ml на MPA в петриеви блюда. Ако е необходимо да се използва селективна среда, дозата на инокулация се увеличава (0,3-0,5 ml). Получената течност в приемника може да се използва за заразяване на животни (например при изследвания, провеждани за откриване на вируси, рикетсии и др.).
Устройството на Дяконов също се основава на улавяне на бактерии в течност, през която се пропуска въздух.
Апаратът PAB-1 е предназначен за бактериологично изследване на големи обеми въздух за кратък период от време. Въздушните проби се получават при скорост 125-150 l / min. Принципът на действие на устройството се основава на улавяне на микроорганизми върху електрод с противоположен заряд. Високата скорост на вземане на проби от въздуха в това устройство и възможността за засяването му върху различни хранителни среди е важна за откриването на патогенни и опортюнистични бактерии (например Pseudomonas aeruginosa в хирургически отделения и др.).
Апаратът на Кротов. Действието се основава на принципа на издухване на струя въздух върху средата в петриевите блюда. Апаратът се състои от три части: блок за вземане на проби от въздух, ротаметър и електрическа част на захранващия механизъм.
Тестовият въздух се засмуква в слота на уреда с помощта на центробежен вентилатор, въртящ се със скорост 4000-5000 rpm и удря повърхността на отворена петриева паничка със среда. Микроорганизмите във въздуха се отлагат върху хранителен агар. За равномерно разпределение на микроорганизмите по цялата повърхност масата с чашата върху нея се върти. Въздухът се изхвърля от инструмента през въздушна тръба, която е свързана с ротаметър, който показва скоростта, с която въздухът се изтегля през инструмента.
Недостатъкът на устройството на Кротов е, че има нужда от електричество, така че не може да се използва при всякакви условия.
Първият ден на изследването
Взетите проби се поставят в термостат при 37°С за 18-24 часа.
Втори ден на изследване
Съдът се изважда от фурната и колониите се преброяват. Бактериалното замърсяване на въздуха се изразява с общия брой микроби в 1 m3 от него.
Плащане. Например, 125 литра въздух са преминали за 10 минути, а на повърхността са израснали 100 колонии.
За да се определи Staphylococcus aureus, оградата се прави върху жълтъчно-солен агар. Плаките с инокулации се инкубират в термостат при 37 ° С в продължение на 24 часа и се инкубират при стайна температура в продължение на 24 часа, за да се разкрие пигментът. Подозрителни колонии на S. aureus подлежат на по-нататъшна идентификация (вж. глава 14).
В детските заведения въздухът се проверява за салмонела. За да направите това, въздухът се инокулира в плоча с бисмут-сулфитна агарна среда.
Откриването на патогенни бактерии и вируси във въздуха в помещенията се извършва по епидемиологични показания. За идентифициране на причинителите на туберкулозата те използват устройството POV; средата на Школникова се използва като среда за улавяне.
30. Оценява условията на труд и определя класа условия на труд според степента на опасност и опасност от работата на зъболекаря, ако съдържанието на метали във въздуха на работната зона надвишава ПДК 2,5 пъти; концентрацията на аерозолите с фиброгенно действие е ... пъти по-висока от ПДК и т.н.
Първата степен на 3-ти клас (нисък, умерен риск) е значително превишаване на параметрите на максимално допустимите концентрации (ПДК) (с 1,1-3 пъти). Създава условия
за развитието на заболявания могат да настъпят обратими функционални промени.
3.2. Втора степен от 3-ти клас (среден, значителен риск) - превишаване на параметрите на ПДК с 3,1-5 пъти. Благоприятства развитието на трайни функционални нарушения, увеличаване на временната неработоспособност, повишаване на общата заболеваемост, появата на първоначалните явления на професионалната патология.
3.3. Трета степен от 3-ти клас (висок риск) - превишаване на параметрите на ПДК с 5,1-10 пъти. Това води до развитие на лека професионална патология, нарастване на хронична обща соматична патология (неспецифичното влияние на вредните фактори върху образуването на болка при предразположени лица, при наличие на латентни анатомични и физиологични дефекти) и временна нетрудоспособност.
3.4. Четвърта степен от 3-ти клас (много висок риск) - превишаване на параметрите на ПДК с повече от 10 пъти. Води до изразена форма на професионални заболявания, значително увеличаване на хроничната непрофесионална патология.
4-ти клас: опасни (екстремни) условия на труд (опасни, свръхвисоки рискови) - са по-чести при извънредни ситуации, допринасят за развитието на остри професионални заболявания.
31. Определете класа условия на труд по тежест и интензивност на трудовия процес на зъболекар, ако се извършват стереотипни работни движения до ... пъти на смяна и др.
при локално натоварване. 1-ви клас - до 20 000, 2-ри клас - до 40 000, клас 3.1 - до 60 000, клас 3.2 - над 60 000
при регионално натоварване. 1-ви клас - до 10 000, 2-ри клас - до 20 000, 3.1 клас - до 30 000, 3.2 клас - над 30 000
1. Определяне на свободен активен хлор (йодометричен метод)
Когато се въведе във вода, хлорът се хидролизира, образувайки хипохлорна и солна киселина.
Cl2 + H2O HOCl + HCl
Получената хипохлорна киселина се дисоциира в хипохлоритен йон OCl - и водороден йон H +.
Хлорът се използва широко за дезинфекция на отпадъчни води в системи за циркулация на вода, както и преди да бъде изхвърлен след пречистване в канализацията или водоема. При изхвърляне на твърди вещества в резервоар след пълно биологично третиране, съдържанието на остатъчен свободен активен хлор не трябва да надвишава 2,5 mg / dm 3.
Същността на метода... Когато анализираната вода се подкисели и към нея се добави калиев йодид, всички изброени по-горе вещества отделят йод:
Cl 2 + 2J - = J 2 + 2Cl -
НClО + 2J - + H + = J 2 + Cl - + H 2 O
ClO - + 2H + + 2J - = J 2 + Cl - + H 2 O
NH 2 O + 2H + + 2J - = J 2 + NH 4 + + Cl -
Освободеният йод се титрува с натриев тиосулфат в присъствието на нишесте. Съдържанието на активен хлор се изразява в mg / dm 3 като хлор. По отношение на хипохлорна киселина, хипохлоритни йони, монохлорамин, това изразяване на резултатите от анализа е произволно, т.к. един мол от тези вещества освобождава два йодни атома и следователно съответства на 2 мола активен хлор, т.е. резултатите са твърде високи.
Реагенти
Натриев тиосулфат, 0,01 N. решение;
Калиев йодид, оцетна киселина, 30% разтвор;
Нишесте, 0,5% разтвор.
Напредък на определянето. 50 ... 100 ml анализирана вода се изсипват в конична колба, снабдена със шлифована стъклена запушалка, добавят се 0,5 g калиев йодид и 10 ml оцетна киселина. След 5 минути освободеният йод се титрува с 0,01 N. разтвор на натриев тиосулфат (със съдържание на активен хлор над 1 mg / dm 3) или 0,005 N. разтвор на натриев тиосулфат (със съдържание на активен хлор от 0,1 до 1 mg / dm 3). В края на титруването се добавят 1-2 ml разтвор на нишесте.
![]()
където а- обем на разтвора на натриев тиосулфат, изразходван за титруване, cm 3;
ДА СЕ- корекционен коефициент за довеждане на концентрацията на разтвора на натриев тиосулфат точно до 0,01 N;
V- обемът на анализираната вода, cm 3;
0,355 е количеството хлор, еквивалентно на 1 ml 0,01 N. разтвор на натриев тиосулфат, mg.
"Свободен активен хлор" и "свързан активен хлор"
Вещества, комбинирани понятия "активен хлор" - са силни окислители Cl 2; HClO и ClO - и "свързаният хлор" са относително слаби окислители NH 2 Cl; NHCl 2 и NCl 3, образувани по време на хлорирането на отпадъчни води, съдържащи амониеви йони, амоняк. Последващото поведение на всяко от тези вещества при смесване на хлорирани отпадъчни води с други отпадъчни води, при преминаване през тръби, варира значително, така че понякога са необходими допълнителни разделяния.
По отношение на "свободния активен хлор" те обикновено се задоволяват с определянето на общото съдържание: Cl 2 + HClO + ClO - и за да се намери съдържанието на всеки от хлорамините, е необходимо да се извършат определения, както следва .
Същността на метода... В неутрална среда (рН = 6,9) свободният активен хлор (Cl 2; HClO и ClO -) незабавно реагира с индикатора N, N / - диетил-n-фенилендиамин, образувайки червени съединения.
Монохлораминът и дихлораминът не реагират с индикатора при тези условия. Свободният активен хлор се титрува с разтвор на сол на Мор. След това в разтвора се въвежда много малко количество калиев йодид, чието каталитично действие води до бързо взаимодействие на монохлорамин и индикатора с образуването на същия червен цвят, който се титрува с разтвор на сол на Мор. След това се въвежда в излишък калиев йодид и дихлораминът влиза в реакцията, която се определя чрез същото титруване. Ако отпадъчната вода съдържа азотен трихлорид NCl 3, тя ще бъде частично идентифицирана като дихлорамин NHCl 2.
Първото определяне трябва да се извърши много бързо при pH 6,9 (или малко по-високо), така че монохлорамин NH 2 Cl да не влезе в реакцията. Необходими са 2 минути, за да реагира напълно; ако разтворът е с повишена температура - 1 мин.
Реагенти
N,N-диетил-n-фенилендиамин, сулфатна сол. 0,15 g диетил-n-фенилендиамин сулфатна сол се разтварят в дестилирана вода, която не съдържа хлор, в която се добавят 2 cm 3 от 10 % (обемно) разтвор на сярна киселина и 2,5 cm 3 от 0,8 % разтвор на EDTA ... Разтворът се разрежда до 100 cm 3 и се съхранява в желязна стъклена бутилка;
Фосфатно буфериран физиологичен разтвор, pH = 6,9. 48,4 g Na2HPO4 се разтварят в дестилирана вода. 2H 2 O и 30 g KH 2 PO 4, добавете 100 cm 3 от 0,8% разтвор на EDTA и разредете до 1 dm 3;
Стандартен разтвор на сол на Мор Fe (NH 4) 2 (SO 4) 2. 6H 2 O, 1 cm 3 от който съответства на 0,1 mg хлор. 1 cm 3 от 25% (обемно) сярна киселина предварително се въвежда в дестилирана вода, след което в нея се разтварят 1,106 g сол на Мор и се разрежда до 1 dm 3;
Калиев йодид. За да приготвите 0,5% разтвор, разтворете 0,5 g KI в 100 cm 3 дестилирана вода. За да приготвите 10% разтвор, разтворете 10 g KI в 100 cm 3 дестилирана вода.
Напредък на определянето.
1. Определяне на свободен активен хлор. Първо, 5 cm 3 от фосфатен буферен разтвор (pH = 6,9) и 5 cm 3 от разтвор на диетил-n-фенилендиамин сулфатна сол се изсипват в колба за титруване, оборудвана със смляна запушалка, смесват се, 100 cm 3 от анализирания пробата се въвежда и веднага се титрува с разтвор на соли на Мор до пълно обезцветяване.
2. Определяне на монохлорамин. След определяне на свободния активен хлор към разтвора се добавя 1 cm 3 от 0,5% разтвор на калиев йодид, разбърква се и се титрува с разтвор на сол на Мор до пълно обезцветяване.
3. Определяне на дихлорамин. След определяне на монохлорамин се добавят 10 cm 3 от 10% разтвор на калиев йодид, разбърква се, оставя се да престои 2 минути и се титрува с разтвор на сол на Мор до промяна на цвета.
Предполага се, че общата концентрация на активен хлор не надвишава 4 mg / dm 3. В противен случай вземете по-малък обем на пробата и инжектирайте дестилирана вода за разреждане, преди да въведете анализираната проба в подготвителната смес.
![]() , (2)
, (2)
където V 1 е обемът на разтвора на сол на Мор, изразходван при първото, второто или третото титруване, cm 3;
V е обемът на пробата, взета за анализ, cm 3;
0,1 е количеството активен хлор, съответстващо на 1 cm 3 разтвор на сол на Мор, mg.
2. Определяне на съдържанието на хлор
Пречистването на отпадъчни води с хлор или разтвор на белина е един от най-разпространените, сравнително евтини начини за дезинфекция и пречистване на отпадъчни води от замърсяване с органични вещества. Но тъй като обикновено DM съдържа вещества, реагиращи с хлор и вещества, взаимодействащи с него много бавно или непълно, както и органични вещества, които изобщо не се окисляват от хлора, определянето на окисляемостта на отпадъчните води не предоставя достатъчно данни, за да се направят заключения за това как водата ще бъдат хлорирани. Ето защо, преди да се вземе решение за пречистване на сухо вещество чрез хлориране, то е специално изследвано. В този случай е необходимо да се определи скоростта, с която протичат реакциите между веществата, съдържащи се във водата и хлора (окислителни и заместващи реакции с хлор), дали достигат края, какъв излишък от добавен хлор е необходим, за да за да протече реакцията до желаната степен за даден период от време. На тези въпроси може да се отговори чрез определяне на хлорния капацитет на отпадъчните води по така наречения диаграматичен метод.
Хлорът третира както филтрирана, така и утаена вода, и заедно със съдържащите се в него суспензии.
Напредък на определянето.Избират се няколко порции от анализираната отпадъчна вода с еднакъв обем и се поставят в съдове със смлени запушалки, в които се третират с различни количества хлорна вода (или разтвор на белина), като първата порция е най-малкото количество. , втората порция е 2 до 3 пъти по-голяма и т.н. и т.н. Препоръчва се провеждането на две серии от подобни експерименти, като се променя продължителността на лечението. Първата серия CB проби се третират с различни количества хлор за много кратко време, например 5 минути. Резултатите от тези експерименти показват наличието на вещества в DM, които бързо реагират с хлора. Втората серия от проби се обработва толкова дълго, колкото процесът на хлориране ще се проведе в предложената пречиствателна станция (обикновено 1-2 часа). След изтичане на планираното време се определя количеството нереагирал хлор във всеки разтвор (чрез йодометричен метод) и се начертава диаграма чрез начертаване на количеството хлор, въведен във всеки разтвор по абсцисната ос, започвайки от най-малкия, а по ординатата - съответното количество от останалия хлор и комбинирайте получените точки от кривата (фиг. 1).